黄 健,黄志明,包永忠,单国荣,翁志学
(浙江大学聚合反应工程国家重点实验室,浙江杭州310027)
引 言
浓缩分离是重要的化工单元操作,采用温敏性水凝胶进行浓缩分离则是新兴的浓缩分离技术,具有低成本、低能耗、易再生、无需高温或高压、操作简单、对生物分子无害等优点[1].聚(N-异丙基丙烯酰胺)(PNIPA)水凝胶是一种典型的温敏性水凝胶,在其低临界溶解温度(LCST)附近体积会发生突变,因而广泛应用于物料分离、固定化酶、药物释放等领域[1 3].Kayaman等[4]曾利用PNIPA凝胶浓缩分离蛋白质;Champ等[5 6]用聚(N 异丙基丙烯酰胺 丙烯酸)水凝胶浓缩细菌和右旋糖苷蓝溶液;Zhuang等[7]则采用温敏性聚(N 异丙基丙烯酰胺-2-丙烯酰胺-2-甲基磺酸丙酯)水凝胶浓缩牛血清蛋白溶液,分离效率达80%以上.以溶胀率和分离效率表征凝胶浓缩分离的效果,数值越大,对分离浓缩过程就越有利.通常增加凝胶交联密度可提高分离效率,但溶胀率却显著下降[4 5],两者难以兼顾.
本文采用亲水/亲油复合交联剂,通过反相悬浮法合成表面强化交联的珠状PNIPA水凝胶,并以聚乙二醇(PEG)模拟生物大分子,考察水凝胶的温敏和浓缩分离性能,以期在溶胀率损失不大的前提下提高凝胶分离效率.
1 实验部分
1.1 原料
N 异丙基丙烯酰胺(NIPA),AcrosOrganics公司,正己烷重结晶提纯;引发剂,过硫酸铵(APS),宜兴市第二化学试剂厂,分析纯;促进剂,N,N,N′,N′, 四甲基乙二胺(TEMED),上海前进化学试剂厂,纯度≥98%;交联剂,N,N′ 亚甲基双丙烯酰胺(BIS),纯度≥98%,瑞士Fluka化学公司;二乙烯苯(DVB),昆山年沙助剂厂,分析纯;分散剂,失水山梨糖醇月桂酸单酯(Span20),上海国药集团化学试剂有限公司,分析纯;正己烷,上海国药集团化学试剂有限公司,分析纯;聚乙二醇(PEG,相对分子质量分别为4000、6000、10000和20000),上海国药集团化学试剂有限公司,分析纯.
1.2 珠状凝胶的合成
在500ml四口夹套反应釜中加入计量的NIPA单体、BIS和DVB交联剂、Span20分散剂、正己烷以及去离子水,通氮排氧,搅拌预分散30min.然后加入定量的APS引发剂和TEMED促进剂,在20℃下反应6h后结束反应.过滤、洗涤、真空干燥,得到白色珠状树脂.
1.3 性能表征
1.3.1 颗粒形态
采用PHILIPSXL30型扫描电子显微镜(SEM)观测干态凝胶的颗粒形态,扫描电镜工作电压为10kV.
1.3.2 溶胀率
称取0 5g干凝胶置于20ml去离子水中,吸水平衡后,用孔径为154μm的尼龙布袋滤去剩余的去离子水并称量,按式(1)计算求得溶胀率(RS).RS=WS/Wd(1)式中 WS为吸水饱和后凝胶的质量,Wd为干凝胶的质量.
1.3.3 浓缩分离效率
在25℃下称取0.05g左右的干凝胶置于5ml待浓缩PEG水溶液(浓度为c0、质量为m0)中,待凝胶充分溶胀后取出凝胶,称量浓缩后PEG水溶液的质量m,采用2WA J型阿贝折射仪(上海光学仪器股份有限公司)在25℃下测定溶液的折光指数,对照标准曲线得到溶液浓度c.在理想情况下,水凝胶只吸收水不吸收溶质,此时分离效率为100%;若待测溶液浓缩前后的浓度不变,则凝胶的分离效率为0.因此浓缩分离效率(ES)可定义为[4]:
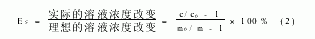
2 结果与讨论
采用反相悬浮聚合法制备PNIPA水凝胶,由于交联剂DVB的疏水性,不易扩散进入反应液滴内部,因而在凝胶粒子形成过程中起到强化表面交联的作用[8],最终得到表面强化交联的凝胶粒子.
2/1 颗粒形态
图1为PNIPA凝胶粒子在干态时的颗粒SEM照片.由图1可见,制备PNIPA凝胶呈规整球形,且表面致密.这是因为聚合温度(20℃)低于PNIPA的低临界溶解温度,此时PNIPA链段可溶于水,因而这种反相悬浮聚合属于珠状悬浮聚合成粒机理[9],得到的聚合物颗粒为致密结构.
2.2 温度敏感性能
图2为凝胶的溶胀率随温度的变化曲线和微分曲线.从图2可以看出,PNIPA凝胶在低温下溶胀吸水,高温下收缩脱水,表现出显著的温敏性.将温敏性凝胶的LCST定义为溶胀率变化最大时的温度[10],从图上微分曲线可以看出制备的凝胶的LCST在32℃左右.这种温敏相转变现象是由PNIPA水凝胶链段内部的亲水/疏水性平衡所决定的[10].PNIPA聚合物同时含有亲水基团(CONH)和疏水基团[CH(CH3)2],表现出双亲性.低温下PNIPA链段的亲水性占优,容易克服凝胶弹性自由能引起的回复力和分子链间的氢键作用力,吸水溶胀;但高温下凝胶链段的疏水性增强,导致凝胶塌陷收缩.
2.3 浓缩分离效率
PEG原料易得,相对分子质量分布窄,不同相对分子质量的PEG可模拟不同大小的蛋白质分子,操作简单,不失活,且与实际蛋白质分子的实验结果相近[11],实验重复性好,因此本文以PEG为溶质分子考察凝胶的浓缩分离性能.
2.3 .1 折光指数的标准曲线
PEG溶液的折光指数与相对分子质量、温度和溶液的浓度有关.在25℃下测定不同相对分子质量PEG、不同浓度水溶液的折光指数,得到如图3所示的标准曲线.

由图3可知,PEG溶液的折光指数与浓度呈线性关系,对图中实验点进行线性拟合得关联式:Y=A+BX,式中Y为折光指数,X为PEG浓度.结果参数列于表1.

由表1可知,参数A基本不随PEG分子量而变,参数B随PEG分子量的增大略有增大.
2.3.2 PEG浓度和相对分子质量的影响
25℃时以PNIPA水凝胶浓缩分离不同浓度、不同相对分子质量PEG的水溶液,浓缩分离效率的变化如图4所示.由图可见,随着PEG相对分子质量的减小和水溶液浓度的增大,水凝胶对PEG/水的浓缩分离效率下降.根据温敏性凝胶浓缩分离机理[1]:在温度低于LCST时,溶质大分子无法进入凝胶孔洞,而溶剂小分子却能自由地渗透入凝胶网络,残液中大分子溶质的浓度提高,因此这类凝胶的分离提纯效率是溶质相对分子质量的函数,相对分子质量越大,分离效率越高.在凝胶吸水过程中,亲水性PEG分子易吸附在凝胶表面,随着水溶液浓度的增加吸附在凝胶表面PEG分子增多,从而导致浓缩分离效率降低.

2.3.3 交联剂浓度的影响
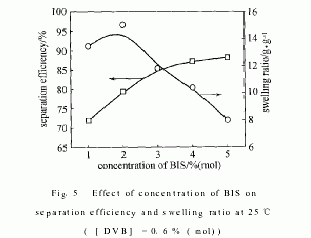
水凝胶是由高分子三维网络与溶液组成的体系,对已确定溶液,凝胶网络的结构对浓缩分离性能起决定作用.本文通过改变交联剂的用量来调节凝胶网络结构,图5和图6分别表示亲水性交联剂BIS和亲油性交联剂DVB的用量对凝胶的分离效率和溶胀率的影响(溶质为PEG10000)."
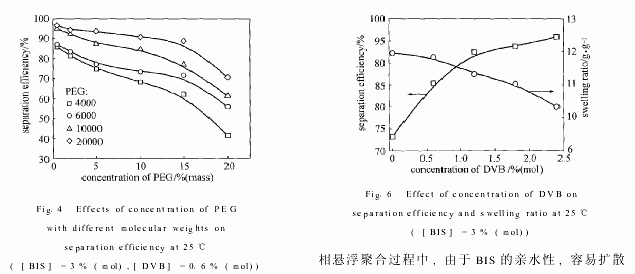
由图5和图6可以看出,随着交联剂用量的增加,凝胶对PEG/水的浓缩分离效率提高,但溶胀率均有不同程度的下降.比较上述两图发现,增加DVB用量对提高凝胶的分离效率要比增加BIS用量更明显,而且凝胶溶胀率下降较少.这是因为两种交联剂本身的亲水/疏水性的差异造成的.在反相悬浮聚合过程中,由于BIS的亲水性,容易扩散并分散于液滴内部参与交联反应,而亲油性交联剂DVB不易扩散入液滴内部,只能在油水界面发生表面交联反应,形成一层疏水表面交联层.随着BIS用量的增加,高分子链段交联点间的网链变短,凝胶结构中的网孔变小,其溶胀率降低.但若BIS用量过少,凝胶内溶胶含量很多,宏观上表现为水溶性,故溶胀率也不高.DVB主要是在凝胶粒子表面进行交联反应,形成疏水性表层,对内部结构影响不大,故增大DVB用量,凝胶溶胀率变化不大.增加BIS用量可使凝胶的网孔变小,导致分离效率增大.值得一提的是,因为BIS交联PNIPA得到的是交联密度不均匀的凝胶[12],网孔大小不均一,因而凝胶的浓缩分离效率增加有限.增加DVB用量,凝胶表面的交联密度增大,表层网孔变小,并且使凝胶表层疏水性增强,使得亲水性PEG分子不易吸附在凝胶上,因此分离效率大大增加.
3 结 论
本文以BIS和DVB为复合交联剂、Span20为分散剂,在较低的温度(20℃)下采用反相悬浮法合成了表面强化交联型珠状PNIPA凝胶粒子.水凝胶粒子表现出显著的温敏特性,其低临界溶解温度在32℃左右.水凝胶粒子对PEG水溶液的浓缩分离性能研究表明,随着溶质PEG相对分子质量的增大或PEG浓度的减小,分离效率提高.增加交联剂BIS的用量,凝胶的分离效率增大,但溶胀率显著降低;而增加DVB用量,凝胶的溶胀率变化不大,但分离效率大大增加,因此说明表面强化交联技术在温敏性凝胶浓缩分离领域很有应用前景. |